Ковалентная связь: понятие, признаки, химический смысл
Важная разновидность связи между атомами
Ковалентная связь наряду с ионной является основным видом химической связи. Она характеризует способность атомов вступать во взаимодействие друг с другом и создавать на уровне электронов плотные оболочки, служащие основой для молекул с совершенно новыми свойствами.
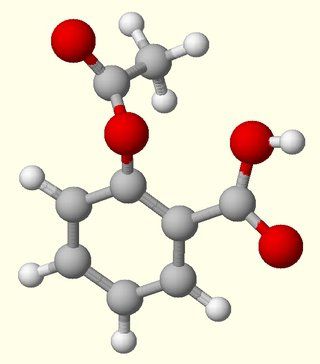
Понятие и химический смысл данного вида химической связи
Согласно пределению, ковалентная связь – это весьма распространенный в природе вид химической связи, при которой происходит объединение электронов атомов, в результате чего образуется общая молекулярная орбиталь. Эта вновь образовавшаяся оболочка позволяет атомам довести число своих электронов до того количества, которое может вместить их внешняя орбита. В результате этого молекула приобретает стабильность и устойчивость.

Основные признаки и свойства
Сам термин «ковалентная связь» означает стремление атомов к взаимодействию с другими атомами, их возможность образовывать устойчивое соединение. Такая связь может возникнуть как между одинаковыми атомами (например, водорода или хлора), так и между разными (например, в молекулах сероводорода, соляной кислоты). В первом случае образуется специфическое электронное облако, элементарные частицы которого, находящиеся на внешней орбитали, начинают обслуживать оба ядра, не обращая внимание на то, являются ли они «своими» или «чужими».
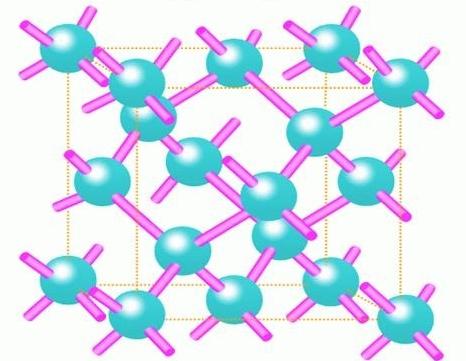
Стремление к снижению затрат энергии
Основной причиной того, что атомы стремятся получить недостающий электрон на свою внешнюю оболочку, является их стремление к снижению энергетических издержек. Ведь уже давно известно, что суммарная энергия молекулы того же водорода гораздо ниже суммы энергий двух атомов этого же элемента. Таким образом, ковалентная связь является естественной реакцией материи на стремление к значительному снижению затрат ресурсов на свое существование.
Еще одно важнейшее следствие
При образовании и дальнейшем существовании данных соединений действует еще одна важная закономерность. Все дело в том, что ковалентная связь опирается на определенные расстояния между атомами в молекуле. Они не могут быть меньше некоторой величины, так как в противном случае система потеряет свою устойчивость, а ее энергия будет стремительно возрастать. Данное свойство активно используется в различных отраслях народного хозяйства, например, в атомной промышленности.
Знаменитое правило Льюиса
Ковалентная связь, свойства которой активно изучаются и в настоящее время, функционирует на основе знаменитого правила октета-дублета, которое было сформулировано в свое время известным химиком Льисом. Согласно его концепции, для образования данного вида связи необходимо такое количество электронов, чтобы внешние оболочки атомов приняли завершенный характер, наподобие того, что представляет собой строение инертных газов. Так, например, в молекуле водорода его составные элементы напоминают гелий, а в молекуле хлора – аргон.
Похожие статьи
- Ковалентная полярная связь: формула, свойства, особенности
- Основные механические свойства твердых тел
- Металлическая связь: электроны в общественной собственности
- Физические и химические свойства углерода
- Что такое электроотрицательность: немного теории
- Сульфид аммония: получение, гидролиз, применение
- Одноатомные спирты. Как получить предельный одноатомный спирт
