Виды химических связей. Как соединить атомы?
Химия – удивительная и, признаться, запутанная наука. Почему-то ассоциируется она с яркими экспериментами, разноцветными пробирками, густыми облаками пара. Но мало кто задумывается о том, откуда же берётся это «волшебство». На самом деле ни одна реакция не проходит без образования соединений между атомами реагентов. Более того, эти «перемычки» иногда встречаются и в простых элементах. Они влияют на способность веществ вступать в реакции и объясняют некоторые их физические свойства.
Какие же бывают виды химических связей и как они влияют на соединения?
Теория
Начинать надо с самого простого. Химическая связь – это взаимодействие, при котором атомы веществ соединяются и образуют более сложные вещества. Ошибочно полагать, что это свойственно только соединениям вроде солей, кислот и оснований – даже простые вещества, молекулы которых состоят из двух атомов, имеют эти «перемычки», если так можно условно назвать связь. Кстати, важно запомнить, что объединиться могут только атомы, имеющие разные заряды (это основы физики: одинаково заряженные частицы отталкиваются, а противоположные – притягиваются), так что в сложных веществах всегда найдётся катион (ион с положительным зарядом) и анион (отрицательная частица), а само соединение всегда будет нейтральным.
Теперь попробуем разобраться в том, как происходит образование химической связи.
Механизм образования
У любого вещества есть определённое количество электронов, распределённых по энергетическим слоям. Самым уязвимым считается внешний слой, на котором обычно находится самое малое количество этих частиц. Узнать их число можно, посмотрев на номер группы (строка с цифрами от одного до восьми в верхней части таблицы Менделеева), в которой находится химический элемент, а количество энергетических слоёв равно номеру периода (от одного до семи, вертикальная строка слева от элементов).
В идеале на внешнем энергетическом слое находятся восемь электронов. Если же их не хватает, атом старается перетянуть их у другой частицы. Именно в процессе отбора необходимых для завершения внешнего энергетического слоя электронов образуются химические связи веществ. Их число может варьироваться и зависит от количества валентных, или неспаренных, частиц (чтобы узнать, сколько их в атоме, нужно составить его электронную формулу). Число электронов, не имеющих пару, будет равно количеству образовавшихся связей.
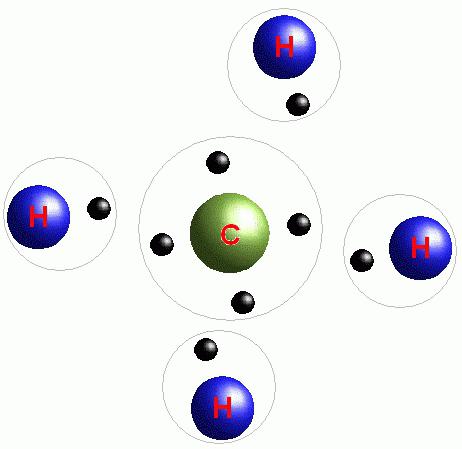
Чуть подробнее о типах
Виды химических связей, образующихся при реакциях или же просто в молекуле какого-то вещества, целиком и полностью зависят от самого элемента. Различают три типа «перемычек» между атомами: ионный, металлический и ковалентный. Последний, в свою очередь, делится на полярный и неполярный.
Для того чтобы понять, какой связью связаны атомы, используют своеобразное правило: если элементы находятся в правой и левой частях таблицы (то есть являются металлом и неметаллом, например NaCl), то их соединение – отличный пример ионной связи. Два неметалла образуют ковалентную полярную связь (HCl), а два атома одного вещества, соединяясь в одну молекулу, – ковалентную неполярную (Cl2, O2). Вышеназванные типы химических связей не подходят для веществ, состоящих из металлов, – там встречается исключительно металлическая связь.
Ковалентное взаимодействие
Как уже упоминалось ранее, виды химических связей имеют определённое влияние на вещества. Так, например, ковалентная «перемычка» очень нестойкая, из-за чего соединения с ней легко разрушаются при малейшем внешнем воздействии, нагревании например. Правда, касается это только молекулярных веществ. Те же, что имеют немолекулярное строение, практически неразрушимы (идеальный пример – кристалл алмаза – соединение атомов углерода).

Вернёмся к полярной и неполярной ковалентной связи. С неполярной всё просто – электроны, между которыми образуется «перемычка», находятся на равном расстоянии от атомов. Но во втором случае они смещаются к одному из элементов. Победителем в «перетягивании» окажется то вещество, электроотрицательность (способность привлекать электроны) которого выше. Определяется она по специальным таблицам, и чем больше разница этой величины у двух элементов, тем более полярной будет связь между ними. Правда единственное, для чего может пригодиться знание электроотрицательности элементов, – определение катиона (положительный заряд – вещество, у которого эта величина будет меньше) и аниона (отрицательная частица с лучшей способностью к привлечению электронов).
Ионная связь
Для соединения металла и неметалла подходят далеко не все типы химических связей. Как уже говорилось выше, если разница в электроотрицательности элементов огромна (а именно так бывает, когда они расположены в противоположных частях таблицы), между ними образуется ионная связь. В этом случае валентные электроны переходят от атома с меньшей электроотрицательностью к атому с большей, образуя анион и катион. Самым ярким примером подобной связи является соединение галогена и металла, например AlCl2 или HF.
Металлическая связь
С металлами всё ещё проще. Им чужды вышеперечисленные виды химических связей, потому что у них есть собственная. Соединять она может как атомы одного вещества (Li2), так и разных (AlCr2), в последнем случае образуются сплавы. Если говорить о физических свойствах, то металлы совмещают в себе пластичность и прочность, то есть они не разрушаются при малейшем воздействии, а просто изменяют форму.

Межмолекулярная связь
Кстати, химические связи в молекулах тоже существуют. Они так и называются - межмолекулярными. Самый распространённый тип – водородная связь, при которой атом водорода заимствует электроны у элемента с высокой электроотрицательностью (у молекулы воды, например).
Похожие статьи
- Химическая связь - понятие и классификация
- Что такое вещество? Строение и свойства веществ
- Углеводороды - это соединения углерода с водородом, не содержащие других элементов. Классификация углеводородов
- Химические свойства аренов. Общая формула и характеристика аренов
- Ковалентная связь: понятие, признаки, химический смысл
- Сернистый газ — физические свойства, получение и применение
- Металлическая связь: электроны в общественной собственности
