Химические свойства этилена. Формула этилена

Непредельные углеводороды с двойной химической связью в молекулах относят к группе алкенов. Первым представителем гомологического ряда является этен, или этилен, формула которого: C2H4. Алкены часто называют олефинами. Название является историческим и возникло в 18-м веке, после получения продукта взаимодействия этилена с хлором – этилхлорида, имеющего вид маслянистой жидкости. Тогда этен и назвали маслородным газом. В нашей статье мы изучим его химические свойства, а также получение и применение в промышленности.
Взаимосвязь между строением молекулы и свойствами вещества
Согласно теории строения органических веществ, предложенной М. Бутлеровым, характеристика соединения полностью зависит структурной формулы и вида связей его молекулы. Химические свойства этилена также определяются пространственной конфигурацией атомов, гибридизацией электронных облаков и наличием в его молекуле пи-связи. Два негибридизованных p-электрона атомов углерода перекрываются в плоскости, перпендикулярной плоскости самой молекулы. Формируется двойная связь, разрыв которой обусловливает способность алкенов к реакциям присоединения и полимеризации.

Физические свойства
Этен – это газообразное вещество, с едва уловимым своеобразным запахом. Оно плохо растворимо в воде, но хорошо растворяется в бензоле, тетрахлорметане, бензине и других органических растворителях. Исходя из формулы этилена С2Н4, его молекулярная масса равна 28, то есть этен немного легче воздуха. В гомологическом ряду алкенов с увеличением их массы агрегатное состояние веществ изменяется по схеме: газ – жидкость – твердое соединение.
Получение газа в лаборатории и промышленности
Нагревая этиловый спирт до 140 °С в присутствии концентрированной серной кислоты, можно получить этилен в лабораторных условиях. Еще один способ – отщепление атомов водорода от молекул алканов. Действуя едким натрием или калием на галогензамещенные соединения предельных углеводородов, например на хлорэтан, добывают этилен. В промышленности наиболее перспективным способом его получения является переработка природного газа, а также пиролиз и крекинг нефти. Все химические свойства этилена - реакции гидратации, полимеризации, присоединения, окисления - объясняются наличием в его молекуле двойной связи.
Взаимодействие олефинов с элементами главной подгруппы седьмой группы
Все члены гомологического ряда этена присоединяют атомы галогенов по месту разрыва пи-связи в своей молекуле. Так, водный раствор брома красно-коричневого цвета обесцвечивается, в результате чего образуется уравнение этилена - дибромэтан:
C2H4 + Br2 = C2H4Br2
Аналогично протекает реакция с хлором и йодом, в ней присоединение атомов галогенов также происходит по месту разрушения двойной связи. Все соединения – олефины могут взаимодействовать с галогеноводородами: хлороводородом, фтороводородом и т.д. В результате реакции присоединения, протекающей по ионному механизму, образуется вещества – галогенопроизводные предельных углеводородов: хлорэтан, фторэтан.
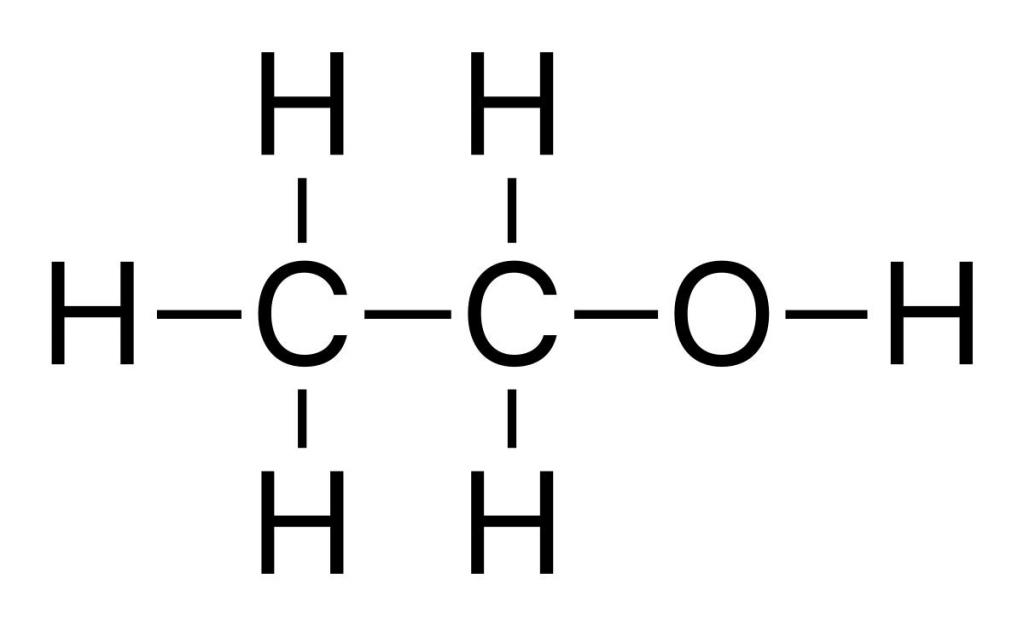
Промышленное производство этанола
Химические свойства этилена часто используют для получения важных веществ, широко применяемых в промышленности и быту. Например, нагревая этен с водой в присутствии ортофосфорной или серной кислот, под действием катализатора происходит процесс гидратации. Он идет с образованием этилового спирта – многотоннажного продукта, получаемого на химических предприятиях органического синтеза. Механизм реакции гидратации протекает по аналогии с другими реакциями присоединения. Кроме того, взаимодействие этилена с водой также происходит в результате разрыва пи-связи. К свободным валентностям атомов углерода этена присоединяются атомы водорода и гидроксогруппа, входящие в состав молекулы воды.
Гидрогенизация и горение этилена
Несмотря на все вышесказанное, реакция соединения водорода не имеет большого практического значения. Однако она показывает генетическую связь между различными классами органических соединений, в данном случае алканов и олефинов. Присоединяя водород, этен превращается в этан. Противоположный процесс – отщепление от предельных углеводородов атомов водорода приводит к образованию представителя алкенов – этена. Жесткое окисление олефинов, называемое горением, сопровождается выделением большого количества тепла, реакция является экзотермической. Продукты сгорания одинаковы для веществ всех классов углеводородов: алканов, непредельных соединений ряда этилена и ацетилена, ароматических веществ. К ним относятся углекислый газ и вода. Воздух в реакции с этиленом образует взрывчатую смесь.

Реакции окисления
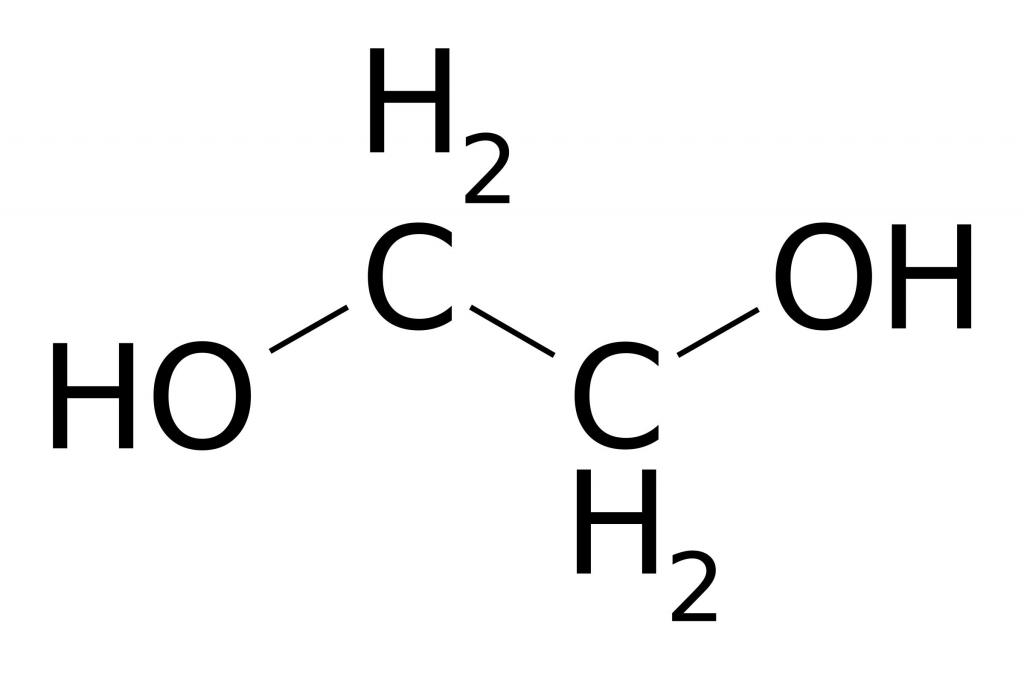
Этен может окисляться раствором перманганата калия. Это одна из качественных реакций, с помощью которой доказывают наличие двойной связи в составе определяемого вещества. Фиолетовая окраска раствора исчезает вследствие разрыва двойной связи и образования двухатомного предельного спирта – этиленгликоля. Продукт реакции имеет широкий спектр применения в промышленности в качестве сырья для получения синтетических волокон, например лавсана, взрывчатых веществ и антифризов. Как видим, химические свойства этилена используются для получения ценных соединений и материалов.
Полимеризация олефинов
Повышение температуры, увеличение давления и применение катализаторов – это необходимые условия для проведения процесса полимеризации. Его механизм отличается от реакций присоединения или окисления. Он представляет собой последовательное связывание многих молекул этилена в местах разрыва двойных связей. Продуктом реакции является полиэтилен, физические характеристики которого зависят от величины n - степени полимеризации. Если она невелика, то вещество находится в жидком агрегатном состоянии. Если показатель приближается к 1000 звеньев, то из такого полимера изготовляют полиэтиленовую пленку, гибкие шланги. Если степень полимеризации превышает 1500 звеньев в цепи, то материал представляет собой твердое вещество белого цвета, жирное на ощупь.

Он идет на изготовление цельнолитых изделий и пластиковых труб. Галогенпроизводное соединение этилена – тефлон обладает антипригарными свойствами и является широко применяемым полимером, востребованным при изготовлении мультиварок, сковород, жаровен. Его высокая способность противостоять истиранию используется в производстве смазок к автомобильным двигателям, а низкая токсичность и толерантность к тканям человеческого организма позволили применять тефлоновые протезы в хирургии.

В нашей статье мы рассмотрели такие химические свойства олефинов, как горение этилена, реакции присоединения, окисления и полимеризации.
Похожие статьи
- Физические свойства алкенов, применение, способы получения
- Ацетилен: химические свойства, получение, применение, меры предосторожности
- Гомологический ряд химических соединений
- Экзотермическая реакция - это процесс, сопровождаемый выделением энергии
- Что такое реакция полимеризации? Реакция полимеризации: уравнение и примеры
- Этиловый спирт. Спирт этиловый медицинский - применение
- Непредельные алкены: формула, свойства, применение
