Что такое число Авогадро?
Закон Авогадро стал настоящим прорывом в теоретической химии и способствовал тому, что гипотетические догадки превратились в великие открытия в области газовой химии. Предположения химиков получили убедительные доказательства в виде математических формул и простых соотношений, а результаты экспериментов теперь позволили делать далеко идущие выводы. Кроме этого, итальянский исследователь вывел количественную характеристику числа структурных частиц химического элемента. Число Авогадро впоследствии стало одной из важнейших констант в современной физике и химии.
Закон объемных отношений
Честь быть первооткрывателем газовых реакций принадлежат Гей-Люссаку, французскому ученому конца XVIII века. Этот исследователь дал миру известный закон, которому подчиняются все реакции, связанные с расширением газов. Гей-Люссак измерял объемы газов перед реакцией и объемы, которые получались в результате химического взаимодействия. В результате эксперимента ученый сделал вывод, известный как закон простых объемных отношений. Суть его в том, что объемы газов до и после соотносятся между собой как целые небольшие числа.
Например, при взаимодействии газообразных веществ, соответствующих, например, одному объему кислорода и двум объемам водорода, получается два объема парообразной воды и так далее.
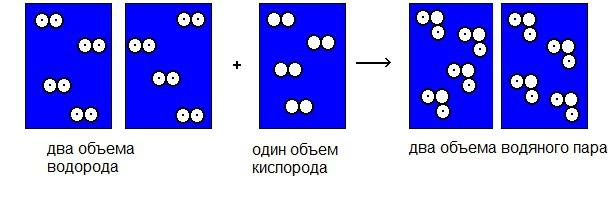
Закон Гей-Люссака справедлив, если все измерения объемов происходят при одинаковых показателях давления и температуры. Этот закон оказался весьма важен для итальянского физика Авогадро. Руководствуясь им, он вывел свое предположение, которое имело далеко идущие последствия в химии и физике газов, и вычислил число Авогадро.
Итальянский ученый
Свою научную деятельность Амедео Авогадро начал с изучения электрохимических явлений. В 1803 году свои работы, посвященные собственно теории электрохимических явлений, он презентовал в Туринскую академию. Позднее его идеи заинтересовали Ампера, которые развил их в полноценную физическую теорию, подкрепленную многочисленными экспериментами. Интересуясь всеми последними открытиями в физике и химии, Авогадро столкнулся с проблемой соотношения объемов различных веществ и количеством заключенных в них молекул. В 1811 году ученый сформулировал предположение, которое объясняло закон Гей-Люссака и давало новый толчок к объяснению многих химических реакций.
Закон Авогадро
В 1811 году Авогадро пришел к пониманию того, что в равных объемах произвольных газов при постоянных значениях температуры и давления содержится одно и то же число молекул.
Закон итальянского исследователя позволил прийти к выводу о количестве атомов в молекулах различных газов. Например, после вывода закона Авогадро подтвердил предположение, что молекулы таких газов, как кислород, водород, хлор, азот, состоят из двух атомов. Также стало возможным установление атомных масс и молекулярных масс элементов, состоящих из разных атомов.
Атомные и молекулярные массы
При вычислении атомного веса какого-либо элемента первоначально за единицу измерения была принята масса водорода как самого легкого химического вещества. Но атомные массы многих химических веществ вычисляются как соотношение их кислородных соединений, то есть отношение кислорода и водорода принималось как 16:1. Эта формула была несколько неудобной для измерений, поэтому эталоном атомной массы приняли массу изотопа углерода - самого распространенного вещества на земле.
На основе закона Авогадро основан принцип определения масс различных газообразных веществ в молекулярном эквиваленте. В 1961 году принимается единая система отсчета относительных атомных величин, в основу которой легла условная единица, равная 1/12 части массы одного изотопа углерода 12С. Сокращенное название атомной единицы массы - а.е.м. Согласно данной шкале, атомная масса кислорода равна 15,999 а.е.м, а углерода - 1,0079 а.е.м. Так возникло новое определение: относительная атомная масса – это масса атома вещества, выраженная в а.е.м.
Масса молекулы вещества
Любое вещество состоит из молекул. Масса такой молекулы выражается в а.е.м, это значение равняется сумме всех атомов, входящих в ее состав. К примеру, молекула водорода имеет массу 2,0158 а.е.м, то есть 1,0079 х 2, а молекулярную массу воды можно вычислить по ее химической формуле H2O. Два атома водорода и единственный атом кислорода в сумме дают значение 18,0152 а.е.м.
Значение атомной массы для каждого вещества принято называть относительной молекулярной массой.
До недавнего времени вместо понятия "атомная масса" использовалось словосочетание «атомный вес». В настоящее время оно не используется, но до сих пор встречается в старых учебниках и научных трудах.
Единица количества вещества
Вместе с единицами объема и массы в химии используется особая мера количества вещества, называемая моль. Эта единица показывает то количество вещества, которое вмещает в себя столько молекул, атомов и других структурных частиц, сколько их содержится в 12 г углерода изотопа 12С. При практическом применении моля вещества следует принимать во внимание, какие именно частицы элементов имеются в виду – ионы, атомы или молекулы. Например, моль ионов H+ и молекул H2 – это совершенно разные меры.
В настоящее время с большой точностью измерено количество вещества в моле вещества.
Мольная масса
Масса одного моля вещества в химии имеет название "мольная масса", эта единица выражается соотношением г/моль. Применяя значение мольной массы на практике, можно видеть, что мольная масса водорода составляет 2,02158 г/моль, кислорода - 1,0079 г/моль и так далее.
Следствия закона Авогадро
Закон Авогадро вполне применим для определения количества вещества при вычислении объема газа. Одинаковое количество молекул любого газообразного вещества при неизменных условиях занимает равный объем. С другой стороны, 1 моль любого вещества содержит неизменное число молекул. Напрашивается вывод: при неизменных температуре и давлении один моль газообразного вещества занимает постоянный объем и содержит равное количество молекул. Число Авогадро утверждает, что в объеме 1 моля газа содержится 6,02 х 1023 молекул.
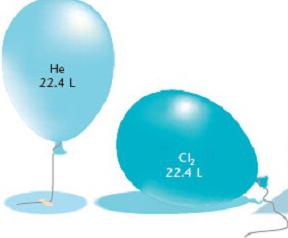
Расчет объема газ для нормальных условий
Нормальные условия в химии – это атмосферное давление 760 мм рт. ст. и температура 0 оC. При этих параметрах экспериментально установлено, что масса одного литра кислорода равна 1,43 кг. Следовательно, объем одного моля кислорода равен 22,4 литра. При вычислении объема любого газа результаты показывали одно и то же значение. Так постоянная Авогадро сделала еще один вывод касательно объемов различных газообразных веществ: при нормальных условиях один моль любого газообразного элемента занимает 22,4 литра. Эта постоянная величина получила название мольного объема газа.
