Молекулярная масса: базовые принципы определения
Молекулярная масса – одно из основных понятий в современной химии. Ее ввод стал возможным после научного обоснования утверждения Авогадро о том, что многие вещества состоят из мельчайших частиц – молекул, каждая из которых, в свою очередь, состоит из атомов. Этим суждением наука во многом обязана итальянскому химику Амадео Авогадро, который научно обосновал молекулярное строение веществ и подарил химии многие важнейшие понятия и законы.

Единицы масс элементов
Первоначально за базовую единицу атомной и молекулярной массы брали атом водорода как наиболее легкого из элементов во Вселенной. Но атомные массы в большинстве своем вычислялись но основе их кислородных соединений, поэтому было принято решение выбрать новый эталон для определения атомных масс. Атомную массу кислорода приняли равной 15, атомную массу самого легкого вещества на Земле, водорода, - 1. В 1961 году кислородная система определения веса была общепринятой, но создавала определенные неудобства.
В 1961 году была принята новая шкала относительных атомных масс, эталоном для которой стал изотоп углерода 12С. Атомная единица массы (сокращенно а.е.м.) составляет 1/12 часть массы этого эталона. В настоящее время атомной массой называют массу атома, которая должна быть выражена в а.е.м.
Масса молекул
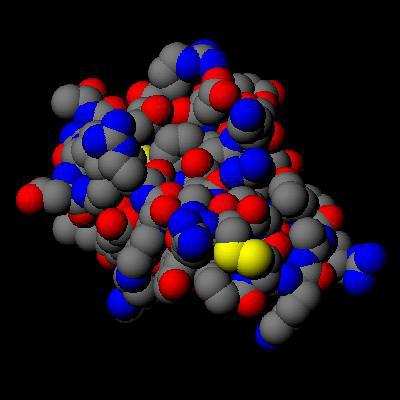
Масса молекула любого вещества равна сумме масс всех атомов, образующих данную молекулу. Самая легкая молекулярная масса газа у водорода, его соединение пишется как Н2 и имеет значение, приближенное к двум. Молекула воды состоит из атома кислорода и двух атомов водорода. Значит, ее молекулярная масса равна 15,994 + 2*1.0079=18.0152 а.е.м. Самые большие молекулярные массы имеют сложные органические соединения – белки и аминокислоты. Молекулярная масса структурной единицы белка колеблется от 600 до 106 и выше, в зависимости от количества пептидных цепей в этой макромолекулярной структуре.
Моль
Одновременно со стандартными единицами массы и объема в химии используется совершенно особая системная единица – моль.
Моль – это количество вещества, которое содержит столько структурных единиц (ионов, атомов, молекул, электронов), столько содержится в 12 граммах изотопа 12С.
При применении меры количества вещества необходимо указывать, какие именно структурные единицы имеются в виду. Как следует из понятия «моль», в каждом отдельном случае следует точно указывать, о каких структурных единицах идет речь – например, моль ионов Н+, моль молекул Н2 и прочее.
Молярная и молекулярная масса
Масса количества вещества в 1 моль измеряется в г/моль и называется молярной массой. Отношение между молекулярной и молярной массой можно записать в виде уравнения
ν = k × m/M, где к – коэффициент пропорциональности.
Нетрудно сказать, что для любых соотношений коэффициент пропорциональности будет равен единице. Действительно, изотоп углерода имеет относительную молекулярную массу 12 а.е.м, а, согласно определению, молярная масса этого вещества равна 12 г/моль. Отношение молекулярной массы к молярной равно 1. Отсюда можно сделать вывод, что молярная и молекулярная масса имеют одинаковые числовые значения.
Объемы газов
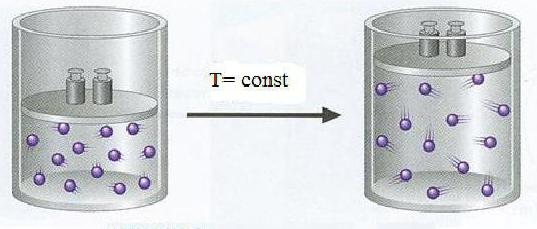
Как известно, все окружающие нас вещества могут пребывать в твердом, жидком или газообразном агрегатном состоянии. Для твердых тел наиболее распространенной базовой мерой является масса, для твердых и жидких – объем. Это связано с тем, что твердые тела сохраняют свою форму и конечные размеры, Жидкие и газообразные вещества конечных размеров не имеют. Особенность любого газа состоит в том, что между его структурными единицами – молекулами, атомами, ионами - расстояние во много раз больше, чем такие же расстояния в жидкостях или твердых телах. Например, один моль воды в нормальных условиях занимает объем 18 мл – приблизительно столько же вмещается в одну столовую ложку. Объем одного моля мелкокристаллической поваренной соли – 58,5 мл, а объем 1 моля сахара больше моля воды в 20 раз. Для газов места требуется еще больше. Один моль азота при нормальных условиях занимает объем, в 1240 раз больший, чем один моль воды.

Таким образом, объемы газообразных веществ существенно отличаются от объемов жидких и твердых. Это обусловлено разностью растояний между молекулами веществ в различных агрегатных состояниях.
Нормальные условия
Состояние любого газа сильно зависит от температуры и давления. Например, азот при температуре в 20 °С занимает объем в 24 литра, а при 100 °С при том же самом давлении - 30,6 литров. Химики учли такую зависимость, поэтому было принято решение сводить все операции и измерения с газообразными веществами к нормальным условиям. Во всем мире параметры нормальных условий одинаковы. Для газообразных химических веществ это:
- Температура в 0°С.
- Давление в 101,3 кПа.
Для нормальных условий принято специальное сокращение – н.у. Иногда в задачах это обозначение не пишется, тогда следует внимательно перечитать условия задачи и привести заданные параметры газа к нормальным условиям.
Расчет объема 1 моля газа
В качестве примера несложно выполнить расчет одного моля любого газа, например азота. Для этого сначала нужно найти значение его относительной молекулярной массы:
Мr(N2)= 2×14=28.
Поскольку относительная молекулярная масса вещества численно равна молярной, то M(N2)=28 г/ моль.
Опытным путем выяснено, что при нормальных условиях плотность азота равна 1,25 г/литр.
Подставим это значение в стандартную формулу, известную со школьного курса физики, где:
- V — объем газа;
- m — масса газа;
- ρ — плотность газа.
Получим, что молярный объем азота при нормальных условиях
V(N2)= 25г/моль : 1,25 г/ литр =22,4 л/ моль.
Получается, что один моль азота занимает 22,4 литра.
Если выполнить такую операцию со всеми существующими газовыми веществам, можно прийти к удивительному выводу: объем любого газа при нормальных условиях равен 22,4 литра. Вне зависимости от того, о каком газе идет речь, какова его структура и физико-химические характеристики, один моль этого газа будет занимать объем 22,4 литра.

Молярный объем газа – одна из важнейших констант в химии. Эта постоянная позволяет решить многие химические задачи, связанные с измерением свойств газов при нормальных условиях.
Итоги
Молекулярная масса газообразных веществ важна для определения количества вещества. А если исследователь знает количество вещества того или иного газа, он может определить массу или объем такого газа. Для одной и той же порции газообразного вещества одновременно выполняются условия:
ν = m/ M ν= V/ Vm.
Если убрать постоянную ν, можно уравнять эти два выражения:
m / M = V/ Vm.
Так можно вычислить массу одной порции вещества и его объем, а также становится известной молекулярная масса исследуемого вещества. Применяя эту формулу, можно легко вычислить соотношение объем-масса. При приведении данной формулы к виду M= m Vm/V станет известна молярная масса искомого соединения. Для того чтобы вычислить это значение, достаточно узнать массу и объем исследуемого газа.
Следует помнить, что строгое соответствие реальной молекулярной массы вещества к той, что найдена по формуле, невозможно. Любой газ содержит массу примесей и добавок, которые вносят определенные изменения в его структуру и влияют на определение его массы. Но эти колебания вносят изменения в третью или четвертую цифру после запятой в найденном результате. Поэтому для школьных задач и экспериментов найденные результаты вполне правдоподобны.
Похожие статьи
- "Преднизолон": отзывы врачей, инструкция по применению и состав
- Динамическая и кинематическая вязкость жидкости. Что это такое?
- Препарат "Нандролон Деканоат": инструкция, механизм действия, отзывы
- Фталаты: что это такое, где содержатся, какой вред наносят здоровью
- Изобарный процесс, связанные с ним уравнения и вывод формулы работы
- Полистирол: формула, свойства, получение, применение
- Как найти молярную массу: проблемы школьников и ученых
