Тип гибридизации атомов
В процессе определения геометрической формы химической частицы важно учитывать, что пары валентных электронов основного атома, включая и те, которые не образуют химической связи, находятся на большом расстоянии друг от друга в пространстве.
Особенности термина
Рассматривая вопрос, касающийся ковалентной химической связи, часто применяют какое понятие, как гибридизация атомных орбиталей. Этот термин связан с выравниванием формы и энергии. Гибридизация атомных орбиталей связана с квантово-химическим процессом перестройки. Орбитали в сравнении с исходными атомами имеют иное строение. Суть гибридизации заключается в том, что тот электрон, который располагается рядом с ядром связанного атома, определяется не конкретной атомной орбиталью, а их совокупностью с равным главным квантовым числом. В основном данный процесс касается высших, близких по энергии атомных орбиталей, имеющих электроны.
Специфика процесса
Типы гибридизации атомов в молекулах зависят от того, как происходит ориентация новых орбиталей. По типу гибридизации можно определить геометрию иона либо молекулы, предположить особенности химических свойств.
Типы гибридизации
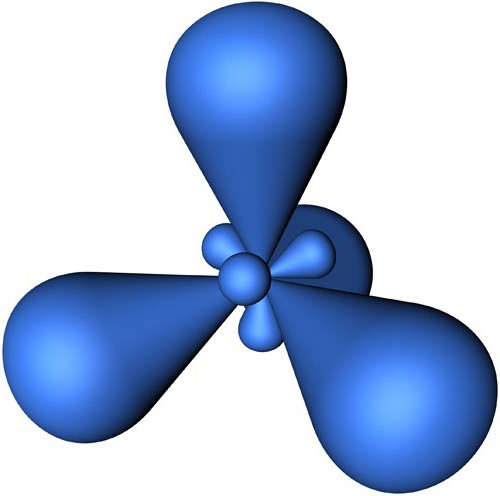
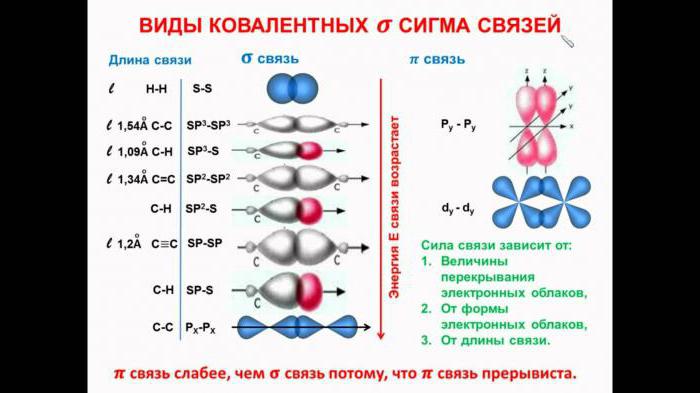
Такой тип гибридизации, как sp, представляет собой линейную структуру, угол между связями составляет 180 градусов. Примером молекулы с подобным вариантом гибридизации является BeCl2.
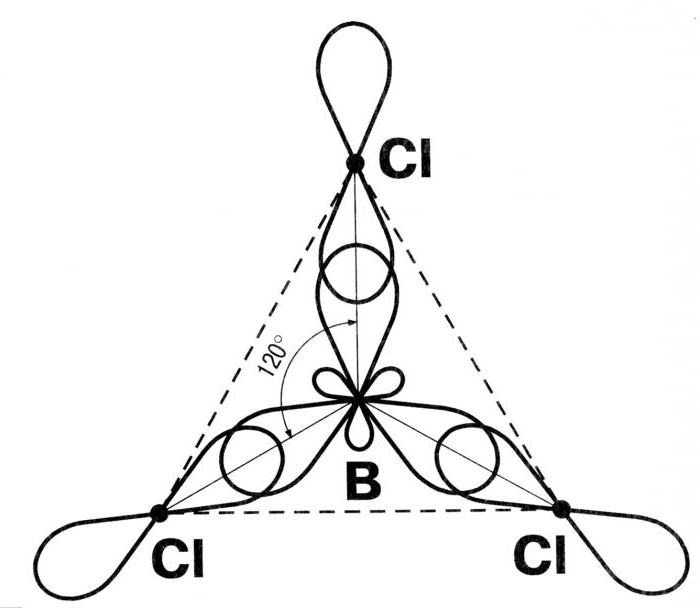
Следующий тип гибридизации – sp2. Молекулы характеризуются треугольной формой, угол между связями составляет 120 градусов. Типичным примером такого варианта гибридизации является BCl3.
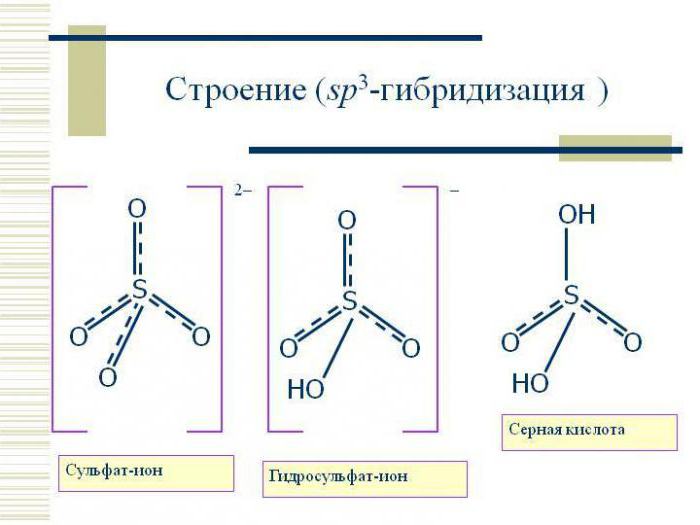
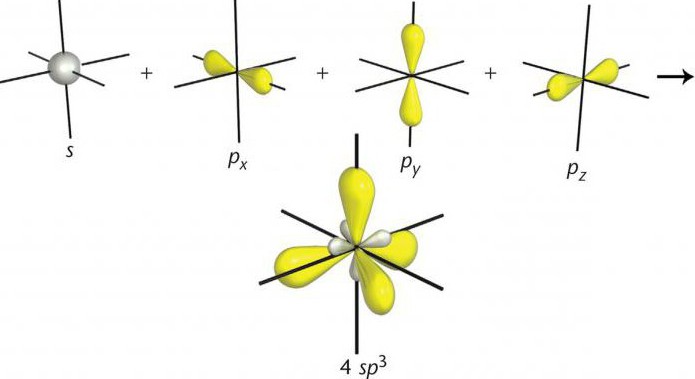
Тип гибридизации sp3 предполагает тетраэдрическое строение молекулы, типичным примером вещества с данным вариантом гибридизации является молекула метана CH4. Валентный угол в таком случае составляет 109 градусов 28 минут.
В гибридизации принимают непосредственное участие не только парные электроны, но и неразделенные пары электронов.
Гибридизация в молекуле воды
К примеру, в молекуле воды между атомом кислорода и атомами водорода существуют две ковалентные полярные связи. Кроме того, сам атом кислорода обладает двумя парами внешних электронов, которые не принимают участия в создании химической связи. Эти 4 электронные пары в пространстве занимают определенное место вокруг кислородного атома. Так как все они обладают одинаковым зарядом, в пространстве они отталкиваются, электронные облака находятся друг от друга на существенном расстоянии. Тип гибридизации атомов в данном веществе предполагает изменение формы атомных орбиталей, происходит их вытягивание и выстраивание к вершинам тетраэдра. В результате молекула воды приобретает угловую форму, между связями кислород-водород валентный угол составляет 104,5o.
Чтобы предсказать тип гибридизации, можно воспользоваться донорно-акцепторным механизмом образования химической связи. В результате осуществляется перекрытие свободных орбиталей элемента с меньшей электроотрицательность, а также орбиталей элемента с большей электрической отрицательностью, на которой находится пара электронов. В процессе составления электронной конфигурации атома учитывается их степень окисления.
Правила выявления вида гибридизации
Для того чтобы определить тип гибридизации углерода, можно использовать определённые правила:
- выявляют центральный атом, вычисляют количество σ-связей;
- ставят в частице степени окисления атомов;
- записывают электронную конфигурацию главного атома в требуемой степени окисления;
- составляют схему распределения по орбиталям валентных электронов, спаривая электроны;
- выделяют орбитали, которые принимают непосредственно участие в образовании связи, находят неспаренные электроны (при недостаточном для гибридизации количестве валентных орбиталей применяют орбитали следующего энергетического уровня).
Геометрия молекулы определяется типом гибридизации. На нее не влияет присутствие пи-связей. В случае дополнительного связывания возможно изменение валентного угла, причина состоит во взаимном отталкивании электронов, образующих кратную связь. Так, в молекуле оксида азота (4) при sp2-гибридизации происходит возрастание валентного угла со 120 градусов до 134 градусов.
Гибридизация в молекуле аммиака
Неразделенная пара электронов оказывает влияние на результирующий показатель дипольного момента всей молекулы. В аммиаке тетраэдрическое строение вместе с неразделенной парой электронов. Ионность связи азот-водород и азот-фтор имеют показатели 15 и 19 процентов, длины определены в 101 и 137 пм соответственно. Таким образом, в молекуле фторида азота должен быть больший дипольный момент, но результаты эксперимента свидетельствуют об обратном.
Гибридизация в органических соединениях
Для каждого класса углеводородов характерен свой тип гибридизации. Так, при образовании молекул класса алканов (предельных углеводородов) все четыре электрона атома углерода образуют гибридные орбитали. При их перекрывании образуется 4 гибридных облака, вытраиваемых к вершинам тетраэдра. Далее их вершины перекрываются с негибридными s-орбиталями водорода, образуя простую связь. Для насыщенных углеводородов характерна sp3-гибридизация.
У ненасыщенных алкенов (их типичным представителем является этилен) в гибридизации принимают участие только три электронных орбитали - s и 2 p, три гибридных орбитали образуют в пространстве форму треугольника. Негибридные p-орбитали перекрываются, создавая в молекуле кратную связь. Этот класс органических углеводородов характеризуется sp2-гибридным состоянием углеродного атома.
Алкины отличаются от предыдущего класса углеводородов тем, что в процессе гибридизации участвуют всего два вида орбиталей: s и p. Оставшиеся у каждого атома углерода два негибридных p-электрона перекрываются в двух направлениях, образуя две кратные связи. Данный класс углеводородов характеризуется sp-гибридным состоянием углеродного атома.
Заключение
Благодаря определению вида гибридизации в молекуле можно объяснить строение разных неорганических и органических веществ, предсказать возможные химические свойства конкретного вещества.
Похожие статьи
- Как выглядит рыба-гибрид? Описание, среда обитания, преимущества перед чистыми формами
- Гибридизация - это что такое? Типы гибридизации
- Гибридные велосипеды: рейтинг и отзывы
- Папилломавирусная инфекция и ее лечение
- Двигатель ЗМЗ-406: описание и технические характеристики
- Гибриды животных и растений: примеры, фото. Гибрид человека и животного
- Массовый отбор в селекции: примеры, преимущества и недостатки
