Озон - это... Определение, свойства, формула
Замечали ли вы когда-то, как приятно дышится после дождя? Этот освежающий воздух обеспечивает озон в атмосфере, который появляется после дождя. Что это за вещество, каковы его функции, формула, а также действительно ли оно полезно для организма человека? Давайте разберемся.
Что такое озон?
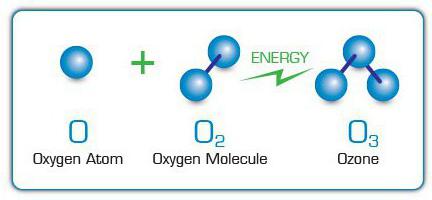
Всем, кто учился в средней школе, известно, что молекула кислорода состоит из двух атомов химического элемента кислорода. Однако этот элемент способен образовывать еще одно химическое соединение – озон. Это название носит вещество, как правило, встречающееся в виде газа (хотя может пребывать во всех трех агрегатных состояниях).
Молекула данного вещества довольно сильно похожа на кислород (О2), однако она состоит не из двух, а из трех атомов - О3.
История открытия озона
Человек, впервые синтезировавший озон – это нидерландский физик Мартин Ван Марум.

Именно он в 1785 г. провел опыт, пропустив через воздух электрический разряд. Получившийся газ не только приобрел специфический запах, но и синеватый оттенок. Помимо этого новое вещество оказалось более сильным окислителем, чем обычный кислород. Так, рассмотрев его влияние на ртуть, Ван Марум обнаружил, что металл немного изменил свои физические свойства, чего с ним не происходило под влиянием кислорода.
Несмотря на свое открытие, нидерландский физик не считал, что озон - это особое вещество. Только через 50 лет после открытия Ван Марума озоном всерьез заинтересовался немецкий ученый Кристиан Фридрих Шенбейн. Именно благодаря ему это вещество получило свое имя – озон (в честь греческого слова, означающего «пахнуть»), а также было более пристально изучено и описано.
Озон: физические свойства
Это вещество имеет ряд свойств. Первым из них является способность озона, как и воды, пребывать в трех агрегатных состояниях.
Нормальное состояние, в котором пребывает озон – газ голубоватого цвета (именно он окрашивает небеса в лазурный цвет) с ощутимым металлическим ароматом. Плотность такого газа - 2,1445 г/дм³.
При снижении температуры молекулы озона образуют сине-фиолетовую жидкость с плотностью 1,59 г/см³ (при температуре -188 °C). Закипает жидкий О3 при -111,8 °C.
Пребывая в твердом состоянии, озон темнеет, становясь практически черным с отчетливым фиолетово-синим отблеском. Его плотность - 1,73 г/см3 (при −195,7 °С). Температура, при которой начинает плавиться твердый озон - это −197,2 °С.
Молекулярная масса О3 – 48 дальтонов.
При температуре в 0 °C озон прекрасно растворяется в воде, причем в десять раз быстрее, чем кислород. Наличие примесей в воде способно еще больше ускорить данную реакцию.
Помимо воды озон растворяется во фреоне, что облегчает его транспортировку.
Среди других веществ, в которых легко растворить О3 (в жидком агрегатном состоянии) - аргон, азот, фтор, метан, углекислота, тетрахлоруглерод.
Также он неплохо смешивается с жидким кислородом (при температуре от 93 К).
Химические свойства озона
Молекула О3 является довольно неустойчивой. По этой причине в нормальном состоянии она существует 10-40 минут, после чего разлагается, образуя небольшое количество тепла и кислород О2. Эта реакция способно произойти и гораздо быстрее, если в качестве катализаторов выступит повышение температуры окружающей среды или понижение атмосферного давления. Также разложению озона способствует и его контакт с металлами (кроме золота, платины и иридия), окислами или веществами органического происхождения.
Взаимодействие с азотной кислотой останавливает разложение О3. Также этому способствует хранение вещества при температуре −78 °С.
Главным химическим свойством озона является его окисляемость. Одним из продуктов окисления всегда является кислород.
При разных условиях О3 способен взаимодействовать практически со всеми веществами и химическими элементами, уменьшая их токсичность путем превращения их в менее опасные. Например, цианиды окисляются им до цианатов, которые намного безопаснее для биологических организмов.
Как добывают?
Чтобы добыть и сохранить столь нестабильное вещество как озон, физические свойства его и химические используются.
Чаще всего для добывания О3 на кислород воздействуют электрическим током. Чтобы разделить получившуюся смесь кислорода и озона, используют свойство последнего лучше сжижаться, чем О2.
В химических лабораториях иногда О3 добывают с помощью реакции охлажденного концентрата серной кислоты с пероксидом бария.
В медицинских учреждениях, использующих О3 для оздоровления пациентов, это вещество получают путем облучения О2 ультрафиолетом (кстати, таким же способом образуется данное вещество в атмосфере Земли под действием солнечных лучей).
Использование О3 в медицине и промышленности
Несложное строение озона, доступность исходного материала для его добывания способствует активному использованию данного вещества в промышленности.
Будучи сильным окислителем, он способен дезинфицировать значительно лучше хлора, формальдегида или окиси этилена, при этом являясь не столь токсичным. Поэтому О3 часто используется для стерилизации медицинских инструментов, оборудования, формы, а также многих препаратов.
В промышленности данное вещество чаще всего используют для очистки или добывания многих химических веществ.
Еще одной отраслью использования является отбеливание бумаги, тканей, минеральных масел.
В химической промышленности О3 не только помогает стерилизовать оборудование, инструменты и тару, но и применяется для обеззараживания самих продуктов (яиц, зерна, мяса, молока) и увеличения их срока хранения. Фактически он считается одним из лучших консервантов для продуктов, поскольку нетоксичен и неканцерогенен, а также прекрасно убивает споры плесени и других грибков и бактерий.

В хлебопекарнях озон применяется для ускорения процесса брожения дрожжей.
Также с помощью О3 искусственно старятся коньяки, производится рафинирование жирных масел.
Как влияет озон на организм человека?
Из-за такой схожести с кислородом бытует заблуждение, что озон – это полезное для организма человека вещество. Однако это не так, поскольку О3 является одним из сильнейших окислителей, способных разрушить легкие и убить каждого, кто чрезмерно вдыхает этого газ. Не зря государственные экологические организации в каждой стране строго следят за концентрацией озона в атмосфере.
Если озон так вреден, то почему же после дождя всегда становится легче дышать?

Дело в том, что одним из свойств О3 является его способность убивать бактерии и очищать вещества от вредных примесей. Во время дождя из-за грозы начинает образовываться озон. Газ этот влияет на токсические вещества, содержащиеся в воздухе, расщепляя их, и очищает кислород от этих примесей. Именно по этой причине воздух после дождя столь свеж и приятен, а небо обретает красивый лазурный цвет.
Эти химические свойства озона, позволяющие ему очищать воздух, в последнее время активно используют для лечения людей, страдающих от различных респираторных заболеваний, а также для очистки воздуха, воды, различных косметических процедур.
Довольно активно сегодня рекламируются бытовые озонаторы, очищающие воздух в доме с помощью данного газа. Хотя эта методика кажется весьма эффективной, пока что учеными недостаточно изучено влияние большого количества очищенного озоном воздуха на организм. По этой причине чрезмерно увлекаться озонированием не стоит.
Похожие статьи
- Что такое жидкий кислород: общая информация
- Озонотерапия: показания и противопоказания, отзывы, описание процедуры, побочные действия
- Карбюратор ОЗОН: устройство, ремонт, настройка
- Интернет-магазины - это... Определение, особенности и виды
- Что такое озоновый слой Земли? Проблемы озонового слоя
- Озоновые дыры: кто виноват?
- Токи Бернара: показания, описание и отзывы
