Нитрат калия: формула, получение, применение
Со многими химическими соединениями мы сталкиваемся очень часто, причем сами того не замечая. Одно из них – это нитрат калия, или индийская селитра. Кристаллический порошок прочно вошел в нашу жизнь: мы его едим (в виде добавок в различные продукты), используем в сельском хозяйстве как очень ценное и полезное удобрение, ну и просто радуемся, глядя на некоторую продукцию, в составе которой он присутствует (фейерверк).
Нитрат калия: формула и описание

Это неорганическое соединение, имеющее формулу KNO3, - соль, образованная азотной кислотой и натрием. Его кристаллы не имеют цвета и запаха. Вещество не летучее, но обладает слабо выраженными гигроскопическими свойствами (то есть способностью впитывать влагу даже из воздуха, но в малых количествах). Нитрат калия практически не токсичен и безвреден для человека и животных. Кристаллы имеют удлиненную игольчатую форму. Очень хорошо растворим в воде (при помощи электролиза из него выделяют калий), а также в гидразине, глицерине, жидком аммиаке. Для очистки нитрата калия иногда используют способ перекристаллизации.
Природные месторождения
Калиевая селитра (KNO3) в естественной среде встречается в основном в виде минерала нитрокалита. Самое крупное его месторождение находится в Индии. Отсюда и второе название соединения – индийская селитра. Минерал образуется в результате длительного процесса разложения азотсодержащих веществ, выделяющийся при этом аммиак связывается специфическими нитробактериями. Данная реакция происходит при высоких температурах воздуха, что и обуславливает распространенность данного минерала в странах с жарким климатом и высокой влажностью.
Химические свойства
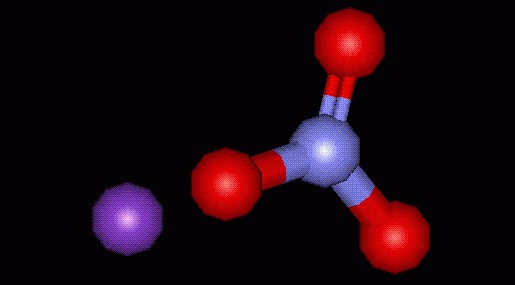
Нитрат калия (формула KNO3) является достаточно сильным окислителем. В измельченном состоянии он очень активно, а иногда и с взрывом реагирует с горючими материалами и некоторыми восстановителями. В реакциях с участием некоторых органических соединений он способен воспламенять и их. Селитры очень неустойчивы и при воздействии температуры разлагаются с образованием нитритов и кислорода. Не исключение и нитрат калия (уравнение: 2KNO3 → 2KNO2 + O2↑). Данное свойство соединения говорит о его весьма высокой пожароопасности, что требует соблюдения специальных правил хранения.
Старейший способ получения
Нитрат калия – это соль, которую начали получать еще в средние века. Для этого использовались большие компостные или навозные кучи, их называли селитряницы. Они делались с использованием известняка, различного строительного мусора, прослоек из хвороста и соломы, чтобы обеспечить доступ кислорода. Сверху, чтобы удержать внутри все выделяющиеся газы, их уплотняли дерном. Когда органика начинала активно разлагаться и гнить, то выделялся аммиак, который не выходил наружу, а оставался в прослойках хвороста и соломы, постепенно подвергаясь процессу нитрификации и трансформации сначала в азотистую, а затем азотную кислоту. Она, в свою очередь, вступала в химическое взаимодействие с находящимся в компостной куче известняком и давала в результате нитрат кальция. Далее его выщелачивали обычной золой (поташем). При этом карбонат кальция выпадал в осадок, и получался раствор нитрата калия. Его использовали в первую очередь для приготовления пороха. Это отражается следующей реакцией:
Ca(NO3)2 + K2CO3 → 2 KNO3 + CaCO3 (в осадок).
Современное получение
Способов получения данного вещества существует несколько. Вот наиболее применяемые и распространенные из них:
- Азотной кислотой нейтрализуют гидроксид калия.
- Абсорбция нитрозных газов гидроксидом калия.
- Конверсионный способ, основанный на разложении нитрата натрия хлоридом калия.
Применение в сельском хозяйстве

Индийская селитра активно используется во многих сферах деятельности человека. Основное направление – сельское хозяйство, где нитрат калия применяется в качестве ценного удобрения. Оно содержит два компонента, которые крайне необходимы растениям для их активного развития. Если они вносятся по отдельности, то взаимно препятствуют друг другу в нормальном усвоении, а если вместе - процесс протекает без каких-либо осложнений. Данное удобрение очень быстро растворяется в почвенном растворе, что тоже является большим плюсом, время воздействия сведено к минимуму. Внесение нитрата калия под плодовые деревья летом и осенью увеличивает их холодостойкость и морозоустойчивость.
Иные области использования
Вторая сфера, где активно применяется нитрат калия, – это получение дымного пороха, который на данный момент в основной своей массе идет на изготовление пиротехнических изделий (военных, специализированных или развлекательных).

Применяется рассматриваемая селитра и при изготовлении твердого ракетного топлива, которое также называют карамельным из-за использования при производстве сахара (сорбита). Оно на 65 % состоит именно из нитрата калия.
Сильные окислительные свойства индийской селитры нашли применение в металлургии, а именно в процессе переработки руд, содержащих никель. Также данное вещество активно используется в области стекольной промышленности, главным образом для осветления хрусталя, повышения прочности продукции. Применяется индийская селитра и при изготовлении эмалей, иной лакокрасочной продукции.
Одна из наименее эффективных и полезных для человека сфер, где используется нитрат калия, – это пищевая промышленность. Там он известен под кодовым названием Е252 (консервант). Его используют для увеличения срока хранения продуктов, так как нитрат калия замедляет процесс размножения бактерий и различных грибков. Активно добавляется это вещество в сыры (твердые, полутвердые, мягкие), колбасы и мясную продукцию, консервированную рыбу, паштеты, изготовленные из гусиной печени. Кроме того, данная добавка улучшает окраску продукта. Достаточно вспомнить красивый, но абсолютно неестественный розовый цвет колбасы.

Важно извлечь информацию следующего характера: добавка Е252 является канцерогеном, то есть веществом, способствующим развитию рака. Несмотря на это, она разрешена к использованию на территории РФ и стран Еврозоны. Этот тот самый случай, когда химия идет против человека.
Похожие статьи
- Калиевая селитра: свойства, получение и применение
- Нитраты - это что такое? Реакции нитратов. Растворы нитратов
- Сульфат аммония: формула, состав, получение и применение
- Дихромат калия: получение, применение, волшебные реакции с участием реагента
- Почему запретили марганцовку и как ее теперь можно приобрести
- Висмута трикалия дицитрат: цены, отзывы, инструкция по применению
- Бертолетова соль: химические свойства, получение и применение
