Автоматия сердца - описание, механизм и особенности
Сердце живого организма — интереснейший продукт эволюции, орган, чья работа основана на взаимодействии гуморальной и нервной систем при сохранении собственной автономии. И пусть сегодня ученым известно практически все, что касается его структуры и деятельности, управлять им достаточно сложно. Однако этому необходимо научиться, что станет отправной точкой в увеличении продолжительности жизни. Автоматия сердца, его метаболизм и связь сокращения с мембранным потенциалом очень важны для медицины. Их изучение и правильное понимание позволяет подбирать более грамотное лечение своим пациентам.
Автоматия пейсмейкеров
Автоматия сердца - это его способность самостоятельно генерировать потенциал действия в фазу диастолы. Это основа автономности данного органа, из-за чего он не зависит от деятельности головного мозга. Причем эволюционно полноценное сердце развилось гораздо раньше головного мозга и центра сердечно-сосудистого тонуса.
Субстрат и причина автоматии сердца заключены в самых фундаментальных механизмах, связанных с работой ионных каналов. Ими формируется разность токов на противоположных сторонах мембраны, которая меняется с течением времени, генерируя импульсный электрический ток. Его проведение по специальным клеткам к потенциал-зависимым тканям является основой сердечной деятельности.
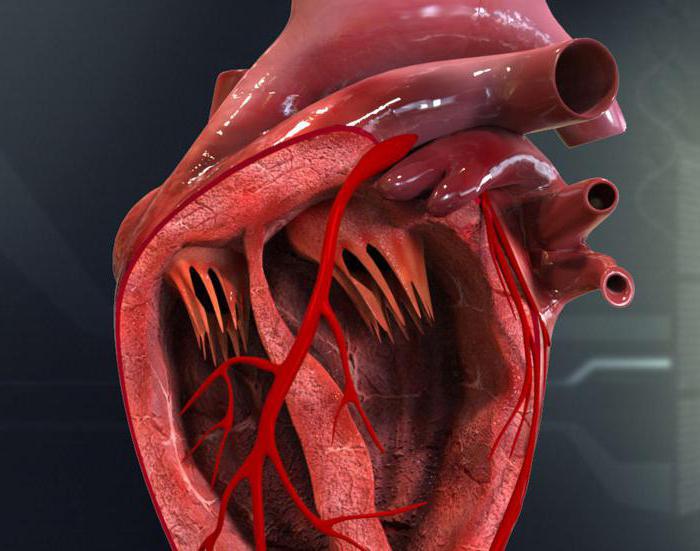
Структура проводящей системы сердца
В сердце, помимо мышечной ткани, имеется собственная система генерации ритма, благодаря чему орган не зависит от контроля головного и спинного мозга. Это система автономна и зависит только от работы ионных каналов атипичных кардиомиоцитов. Они делятся на 3 вида в зависимости от особенностей структуры и функций. Первый вид — пейсмекерные клетки, атипичные Р-кардиомиоциты. Второй вид клеток — проводящие переходные клетки, третий тип — расположенные субэндокардиально клетки волокон Пуркинье и пучка Гиса.
Р-кардиомиоциты — это овальные или округлые клетки, водители ритма, благодаря которым реализуется автоматия сердца. Они в большом количестве находятся в самом центре синусового узла. Небольшое их количество имеется в предсердно-желудочковом узле проводящей системы.
Промежуточные кардиомиоциты имеют продолговатую форму, вытянутые, отличаются малым количеством миофибрилл, но по размеру они меньше сократительных кардиомиоцитов. Они располагаются по периферии синусового и атриовентрикулярного узла. Их задачей является проведение импульса к пучку Гиса и к лежащим между эндокардом и поверхностными слоями миокарда волокнами.
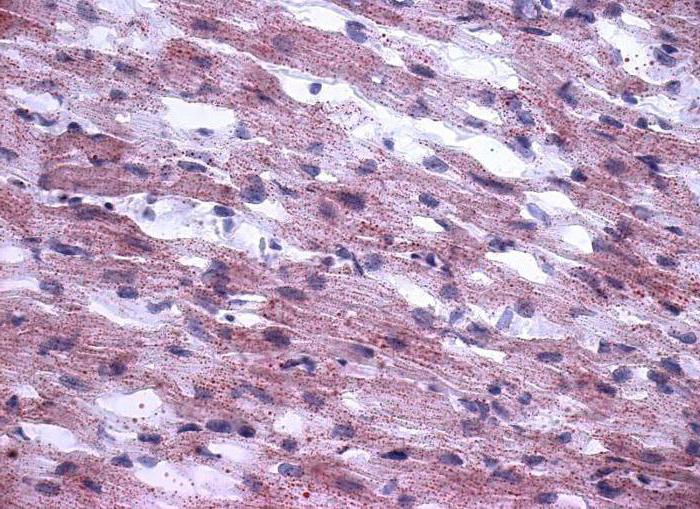
Клетки проводящей системы, локализованные в пучке Гиса и волокнах Пуркинье, имеют особенную структуру и отличаются низкой эффективностью гликолиза за счет преобладания анаэробного его варианта. Они уплощены и длиннее промежуточных кардиомиоцитов, а по размеру чуть больше сократительных клеток. В цитоплазме имеют незначительное количество мышечных волокон. Их задача — соединить узлы автоматии сердца и сократительный миокард, то есть провести импульс от водителя ритма к сердечной мышце.
Нормальный ритм и распространение импульса в сердце
Сокращение сердца — это результат генерации сердечного импульса, потенциала действия пейсмекерных клеток синусового узла. Здесь располагается максимальное количество пейсмейкеров, генерирующих ритм с частотой 60-100 раз в минуту. Он передается по проводящим клеткам до предсердно-желудочкового узла, главной задачей которого является задержка ритма. До АВ-узла возбуждение доходит по пучкам из проводящих кардиомиоцитов, также обладающих автоматизмом. Однако они способны генерировать ритм с частотой 30-40 раз в минуту.
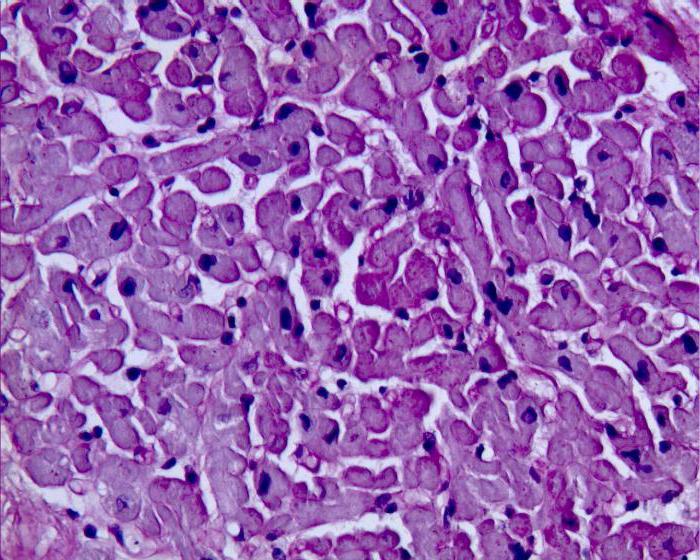
После АВ-узла ритм в норме распространяется по проводящим атипичным кардиомиоцитам к пучку Гиса, автоматизм которого предельно низок — до 20 импульсов в минуту. Затем возбуждение доходит до конечного элемента проводящей системы — волокон Пуркинье. Их способность генерировать ритм еще ниже — до 10 в минуту. Причем основной водитель ритма, то есть синусовый узел, генерирует импульсы намного чаще. И каждое последующее распространение потенциала действия подавляет ритм нижележащих отделов.
Уменьшение способности проводящей системы сердца генерировать ритм высокой частоты от синусового узла к волокнам Пуркинье называется градиентом автоматизма. Этот процесс объясняется уменьшением скорости деполяризации мембраны: в синусовом узле спонтанная медленная диастолическая деполяризация максимально высокая, а по ходу движения к дистальным участкам — наименьшая. Градиент автоматии направлен вниз, что является признаком нормально функционирующей проводящей системы сердца.
Изменение мембранного потенциала пейсмейкеров
В диастолу сердца в пейсмекерных клетках наблюдается следующая ионная картина: в клетке значительно преобладает количество катионов калия над натриевыми ионами. Снаружи клетки концентрация катионов прямо противоположная. При этом потенциал покоя пейсмекерной клетки составляет -60 мВ. Калиевые токи в покое обладают малой эффективностью, так как ионных каналов для калия на мембране очень мало. Это отличает их от сократительных миоцитов, где потенциал покоя составляет примерно -90 мВ.

Работа HCN-каналов и запуск СМДД
Спонтанная медленная диастолическая деполяризация (СМДД), характерная для каждого атипичного кардиомиоцита, приводит к изменению мембранного потенциала и является процессом, ответственным за автоматию сердца. СМДД начинается с работы HCN-ионных каналов. Это так называемые активируемые гиперполяризацией, управляемые циклическими нуклеотидами катионные каналы. ЦАМФ активирует их в момент гиперполяризации, то есть при потенциале покоя, равном -60 мВ. Это значит, что после каждой реполяризации, как только клетка «перезарядилась», и ее мембранный потенциал достиг значения -60 мВ, запускается открытие HCN-каналов. В клетку в результате этого поступают катионы, преимущественно через натриевые каналы.
В результате небольшого натриевого притока мембранный потенциал повысится примерно до -57 мВ. Это является сигналом для активации кальциевых каналов Т-типа, предназначенных для поставки катионов Са2+. Они активируются слабой деполяризацией и называются подпороговыми. Это значит, что повышение мембранного потенциала до -55-57 мВ приведет к открытию транспортных каналов для дальнейшей деполяризации. Эти ионные каналы активируются ионами натрия, расположенными внутри клетки, закачивают некоторое количество кальция в цитоплазму и повышают потенциал до -50 мВ, после чего быстро закрываются.
Работа натрий-кальциевого обменника
Наличие кальция в цитоплазме является сигналом для открытия механизма натрий-кальциевого обменника. Смысл его работы таков: путем активного транспорта в межклеточное пространство выделяются ионы кальция с зарядом 2+, а внутрь клетки поступают Na+ ионы. На один катион кальция в цитоплазму поступает 3 натрий+ иона, что приводит к увеличению заряда мембраны и росту мембранного потенциала до -40 мВ.
Генерация потенциала действия
По достижении потенциала в -40 мВ происходит открытие потенциалзависимых кальциевых каналов L-типа. Они способны работать достаточно долго и приводят к быстрому нарастанию концентрации кальциевых ионов внутри клетки. Это важнейший процесс в работе ионных каналов, так как за счет него происходит лавинообразный рост заряда мембраны, что формирует потенциал действия (ПД). Этот ионный процесс повышает мембранный потенциал до пика на уровне +30 мВ, после чего клетка полностью деполяризована и сгенерировала нужный для работы сердца импульс.
Деполяризация мембраны является активатором не только кальциевого тока, но и калиевого. Однако ионные каналы, которые выделяют ионы калия наружу, работают с задержкой. Потому их выделение происходит на пике формирования ПД. Тогда же кальциевый ток по L-каналам полностью прекращается, а мембранный потенциал снова снижается путем выведения ионов калия против градиента концентрации путем активного транспорта. Заряд мембраны снова падает до -60 мВ, запуская процесс СМДД после уравновешивания изначальных концентраций кальция и натрия.
Природа автоматизма и ее регуляция
Атипичный кардиомиоцит способен выполнять свою функцию благодаря кальциевому току по медленным ионным каналам, в результате чего формируется потенциал действия. Именно этот процесс лежит в основе возбудимости миокарда. В отличие от него, СМДД имеет другое предназначение. Его задача — автоматически запускать начало деполяризации с определенной частотой. Именно наличие фазы СМДД — это природа автоматии сердца, способности спонтанно генерировать возбуждение в пейсмекерных клетках.
Скорость развития СМДД напрямую регулируется соматической вегетативной нервной системой. В покое она минимальна за счет ингибирующего действия блуждающего нерва. Однако это не означает, что автоматия сердца прекращается. Просто стадия СМДД будет длиться больше, что обеспечит более долгую диастолу. Интенсивность метаболических процессов в миокарде и проводящей системе сердца снижается, а орган испытывает меньшую нагрузку.
Эффект ускорения спонтанной медленной диастолической деполяризации достигается влиянием симпатической нервной системы и ее медиатора адреналина. Тогда скорость СМДД повышается, что обеспечивает раннюю активацию натрий-кальциевого обменника и открытие кальциевых каналов медленного типа. Результатом является ускорение частоты ритма, учащение сердцебиения, увеличение энергетического расхода.
Фармакологическое влияние на пейсмейкерную автоматию
Ингибировать механизм автоматии сердца можно и фармакологическим способом. Применяя некоторые лекарственные, наркотические и ядовитые вещества можно ускорить генерацию ритма, замедлить ее или полностью заблокировать. Разумеется, по этическим соображениям ядовитые и наркотические вещества в данной публикации рассматриваться не будут.
Замедлить скорость генерации ритма способны препараты следующих групп: адреноблокаторы и блокаторы кальциевых каналов. Это безопасные лекарственные средства, особенно селективные бета-1-адреноблокаторы. Их механизм действия сводится к инактивации рецептора, к которому в норме присоединяется адреналин.
Блокируя рецептор, препарат устраняет активирующее действие адреналина на скорость генерации импульса, защищая миокард от перерасхода энергии и неэффективной ее растраты. Это очень тонкий и эффективный механизм, а бета-адреноблокаторы значительно увеличили продолжительность жизни многих пациентов с заболеваниями сердца.
Блокаторы кальциевых каналов
Вторая группа веществ отличается более тонким механизмом действия, хотя и очень эффективным. Ими блокируются медленные каналы кальциевого притока, за счет которых формируется потенциал действия. На мембране атипичного кардиомиоцита они экспрессированы в огромном количестве, а потому полная их блокада, которая обернулась бы невозможностью проявления автоматии сердца, невозможна.
Применением препарата достигается лишь некоторое замедление скорости генерации потенциала действия, что помогает уменьшить частоту ритма. Такой механизм очень надежный и позволяет лечить аритмии, используя для этого не субстрат автоматии сердца, а сам потенциал действия. То есть блокаторы кальциевых каналов не влияют на спонтанную медленную диастолическую деполяризацию.
Связь автоматизма сердца и жизнедеятельности
Сердце состоит из мышечной ткани, соединительной и нервной. Последняя имеет в нем наименьшее значение, так как представлена только блуждающим нервом. Соединительная ткань обеспечивает наличие клапанов и поддерживает структуру органа, тогда как мышечная отвечает за все остальное. Именно производными мышечных клеток являются атипичные кардиомиоциты. Это означает, что автоматия сердца, проводящая система сердца и ее мышечная часть являются функциональным целым. Они формируют автономный орган, который способен регулироваться самостоятельно, но не исключает влияние других систем организма.

Такие понятия как автоматия сердца, природа автоматии, градиент автоматии взаимосвязаны и стоят на страже здоровья. Они поддерживают жизнь в организме, обеспечивая постоянное кровоснабжение тканей. Кровь в артериях — это транспортная среда для питательных веществ и связанного кислорода. Благодаря этому реализуется процесс клеточного дыхания и обмена энергией. Это основа функционирования многоклеточного организма, при прекращении работы которой неизбежна его гибель.
Похожие статьи
- Ирригоскопия - это метод исследования кишечника. Как подготовиться к ирригоскопии?
- Где находится сердце у человека? Топография сердца и органов грудной клетки
- Сердечно-сосудистая дистония: симптомы и лечение
- Анатомия сердца. Строение и работа сердца
- Неполная блокада правой ножки пучка Гиса - как лечить?
- Что такое потенциал? Значение, синонимы и толкование
- Боли в сердце: симптомы каких болезней? Ноющая, острая или давящая боль в сердце, что делать?
